C9orf72での RANTing
筋萎縮性側索硬化症 (ALS) 研究で、現在最もホットな遺伝子は C9orf72かもしれません。このブログでも何度か紹介しています。
2011年9月、C9orf72のイントロン領域における GGGGCC 6塩基リピートがフィンランド人 (Finnish) において孤発性 ALS患者の 21.1%を占めることが報告され、大きな衝撃を与えました。その後、さまざまな国における遺伝子変異の頻度の報告が相次いでいますが、国によりかなり状況は異なるようです。
C9orf72について、2013年 2月 20日の Neuron誌に興味深い論文が掲載されました。その論文は同誌の “Previews” で注目の論文として紹介されています。まずは紹介記事を示します。
RANTing about C9orf72
Neuron, Volume 77, Issue 4, 597-598, 20 February 2013
10.1016/j.neuron.2013.02.009Refers to: Unconventional Translation of C9ORF72 GG…
Authors
C9orf72がどのようにして ALSの発症に関与しているかはわかっていませんが、これまで 2つのメカニズムが推測されていました。
① gain of function
筋緊張性ジストロフィーのように noncoding lesionの異常な反復配列がみられる疾患では、機能獲得を起こすことが知られています。こうした疾患では、転写された repeat RNAが核に RNA fociという凝集体を形成します。RNA fociは RNA結合蛋白を独占してしまい、RNA結合蛋白の喪失が最終的に疾患を発症させます。C9orf72患者において RNA fociの存在が報告されています。
② loss of function
C9orf72は、Rab-GTPaseを活性化する GDP/GTP exchange factors (GEFs) である DENN蛋白との構造上の類似性から、小胞輸送に関与しているのではないかと推測されています。C9orf72の機能喪失を支持する知見として、 GGGGCC反復配列を含む転写産物レベルが患者の脳で低下していることが挙げられます。
今回、Ashらにより、第 3の仮説が登場しました。
③ RAN translation
Huntington病や一部の脊髄小脳失調症のように CAGリピートがみられる疾患において、開始コドンを介さないリピート関連翻訳 (repeat-associated non-ATG translation; RAN translation) がみられることが近年報告されました。RAN translationが起きるには、最低 58個の CAGリピートが必要で、RAN翻訳産物は凝集体を形成します。
Ashらは、C9orf72の CCCCGG配列で RAN translationが起こっているか調べるため、poly-(glycine-proline), poly-(glycine-alanine), poly-(glycine-arginine) に対する抗体を作製し、C9orf72変異 ALS患者の神経組織で免疫染色しました。すると、しばしば Cporf72変異 ALS患者で認められる p62陽性/TDP-43陰性封入体と似たような形状・分布で C9RANT陽性神経凝集体が染色されました。
“Previews” ではこのように、非常にわかりやくポイントが示されていました。そして実際の論文は下記です。
Unconventional Translation of C9ORF72 GGGGCC Expansion Generates Insoluble Polypeptides Specific to c9FTD/ALS
Neuron, Volume 77, Issue 4, 639-646, 12 February 2013
10.1016/j.neuron.2013.02.004Referred to by: RANTing about C9orf72
Authors
- Highlights
- C9ORF72-expanded GGGGCC repeat RNA undergoes unconventional translation
- A C9ORF72 RAN translation product accumulates in insoluble inclusions in the brain
- Inclusions are specific to c9FTD/ALS and not in other neurodegenerative disorders
- C9ORF72 RAN translation peptides maybe a potential biomarker and therapeutic target
Summary
Frontotemporal dementia (FTD) and amyotrophic lateral sclerosis (ALS) are devastating neurodegenerative disorders with clinical, genetic, and neuropathological overlap. Hexanucleotide (GGGGCC) repeat expansions in a noncoding region of C9ORF72 are the major genetic cause of FTD and ALS (c9FTD/ALS). The RNA structure of GGGGCC repeats renders these transcripts susceptible to an unconventional mechanism of translation—repeat-associated non-ATG (RAN) translation. Antibodies generated against putative GGGGCC repeat RAN-translated peptides (anti-C9RANT) detected high molecular weight, insoluble material in brain homogenates, and neuronal inclusions throughout the CNS of c9FTD/ALS cases. C9RANT immunoreactivity was not found in other neurodegenerative diseases, including CAG repeat disorders, or in peripheral tissues of c9FTD/ALS. The specificity of C9RANT for c9FTD/ALS is a potential biomarker for this most common cause of FTD and ALS. These findings have significant implications for treatment strategies directed at RAN-translated peptides and their aggregation and the RNA structures necessary for their production.
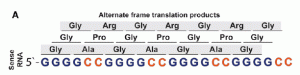
C9orf72において RAN translationがないか調べるため、著者らはまず poly-(glycine-proline), poly-(glycine-alanine), poly-(glycine-arginine) に対するポリクローナル抗体 (抗C9RANT抗体) を作製しました。論文の figure 1Aを見ると、なぜこの組み合わせのポリアミノ酸を調べなければいけないかがよくわかります。”GGGGCC” 反復のフレームシフトによって出来るアミノ酸が変わってくるからですね。。
次に、著者らは作製された抗体を検定し、poly-(glycine-proline) peptideに対する抗体を用いるのが最も良いことを確認しました。
それから、ALSないし前頭側頭葉変性症 (FTLD) 患者の小脳組織を抽出し、Western blot及び dot blotを行いました。その結果、C9orf72変異のある患者ではバンドが検出された一方で、変異のない患者ではバンドは検出されませんでした。
さらに小脳組織から得られた pre-mRNAの塩基配列を調べると、開始コドンと GGGGCC配列の間に複数の終止コドンがあることがわかりました。したがって、GGGGCC配列は開始コドン (ATG) によって翻訳されていないことがわかりました。つまり、GGGGCCは開始コドンを介さない翻訳 (=リピート関連翻訳) が行われていることになります。
続けて免疫組織化学的評価をしました。C9orf72変異 ALSでは、TDP-43陰性ユビキチン陽性ないしユビキチン結合蛋白 (p62, ubiquilin-2) 陽性封入体が出現することが知られています。これらの封入体と、C9RANT抗体陽性の神経細胞質/核内封入体は形態的に似通っていました。抗 C9RANT抗体に反応したのは、灰白質および神経内封入体のみで、血管内皮細胞、平滑筋細胞、白質、グリアでは反応しませんでした。
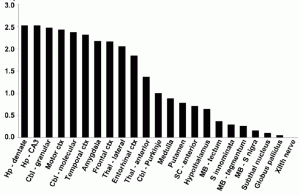
C9RANT陽性封入体が脳内のどこに出やすいか、30症例で調べたのが Figure 2Qです。
C9RANT陽性封入体が最も豊富に見られたのは、p62陽性封入体がみられる小脳でした。しかし、p62陽性封入体とは異なり、外側膝状体や内側膝状体でも検出されました。
C9RANT陽性封入体は、C9orf72変異を伴わない FTLD/ALSや他の変性疾患 (アルツハイマー病、レビー小体病、多系統萎縮症、進行性核上性麻痺、皮質基底核変性症) では検出されませんでした。トリプレットリピート病 (ハンチントン病、脊髄小脳失調症 3型、球脊髄性筋萎縮症) では、p62陽性封入体が検出された一方で、C9RANT陽性封入体は検出されませんでした。
また、C9orf72変異を伴う患者において、骨格筋、末梢神経、後根神経節、心臓、肺、肝臓、脾臓、腎臓、精巣を調べましたが、精巣のセルトリ細胞を除いて、C9RANT陽性封入体は検出されませんでした。
著者らは、C9orf72に対する髄液の immunoassayが進歩すれば、疾患の活動性や進行に対するマーカーとして使えるのではないかと考えております。
C9orf72は ALSにおけるホットトピックスということもあり、どんどんと知見が積み重なっています。今回の C9RANTは、分子メカニズムという観点からはかなり意義のある報告です。しかし、知見が積み重なるにつれてますます問題が複雑化している感もあります。
(2013.3.8 追記 )
ブログ “First Author’s” に、この領域の研究著者による解説が載っていましたので紹介しておきます。