COVID-19とGuillain-Barre症候群/Fisher症候群
COVID-19とGuillain-Barre症候群/Fisher症候群について、最近みかけた論文を備忘録に残しておきます。
①Guillain-Barré syndrome associated with SARS-CoV-2 infection: causality or coincidence? (Lancet Neurol. 2020.4.1 published online)
症例は61歳女性。2020年1月19日に武漢から帰還。発熱や呼吸器症状などなし。1月23日から下肢筋力低下が出現し、四肢筋力低下に進行。神経伝導検査では脱髄を示唆。ギラン・バレー症候群の診断。蛋白細胞乖離あり。1月30日に発熱、咳があり、胸部CTで肺炎像確認。咽頭スワブでのRT-PCRでSARS-CoV-2陽性確認。治療は、Guillain-Barre症候群に対して免疫グロブリン大量静注療法、COVID-19に対してarbidol, lopinavir, and ritonavirが投与された。筋力、呼吸器症状とも改善した。
臨床経過に少し違和感があります。COVID-19感染からしばらくしてGuillain-Barre症候群発症なら納得できるけれど、この症例では神経症状が出てからCOVID-19の症状が出ているからです。ただ、その後に次々と出てきた報告を見ると、COVID-19がGuillain-Barre症候群を合併しうることはほぼ確実と思われます。
②Guillain Barre syndrome associated with COVID-19 infection: A case report. (J Clin Neurosci, 2020.4.15 published online)
症例は65歳男性。急速進行性の四肢麻痺で入院した。患者は入院5日前から急速進行性の両下肢筋力低下があり、入院前日に四肢麻痺となった。両側顔面麻痺も伴っていた。入院2週間前に、咳、発熱、呼吸苦があり、鼻咽頭検体採取、胸部CTの後に、COVID-19と診断されていた。SARS-CoV-2 RT-PCRが陽性だったので、その時にヒドロキシクロロキン、ロピナビル/リトナビル、アジスロマイシンで治療されていた。基礎疾患には糖尿病がありメトホルミンを内服中であった。入院9日目におこなった電気生理検査では、CMAPが低下しており、SNAPは導出されなかった。患者の同意が得られず髄液検査はおこなわなかった。Guillain-Barre症候群のAMSAN (acute motor-sensory axonal neuropathy) と診断した。免疫グロブリン大量療法をおこなった。
イランからの報告です。Guillain-Barre症候群として典型的な経過だと思います。
③Guillain-Barré Syndrome associated with SARS-CoV-2 infection. (IDcases, 2020.4.18 published online)
症例は54歳男性。2日間続く両下肢のしびれ感と筋力低下を自覚した。麻痺は進行し、寝たきりとなった。救急外来では、38.9℃の発熱があり、アモキシシリンやステロイドで改善せず10日持続する乾性咳嗽があった。彼は2日前にクロストリジウム・ディフィシルによる腸炎を2日前に発症したが、治療で改善した。喀痰からはライノウイルスが検出された。またSARS-CoV-2を提出した。著者らの病院に到着したとき、四肢筋力低下 (MMT 2-3程度) があり、腱反射は消失していた。Guillain-Barre症候群の診断で免疫グロブリン大量投与が行われた。著者らの病院でSARS-CoV-2が再検され、前医とともに陽性であることが判明した。ヒドロキシクロロキンが投与された。典型的な症例であり感染制御の観点から、筋電図や髄液検査は行わなかった。症状は改善し、免疫グロブリン投与4日目で人工呼吸器を離脱した。上肢筋力は良くなったが、下肢の筋力低下は残存し、リハビリテーションを継続した。
COVID-19を発症してから5-10日で出現した筋力低下であり、Guillain-Barre症候群として典型的な経過です。
④Guillain-Barre syndrome associated with SARS-CoV-2 (N Engl J Med, 2020.4.19 published online)
5例報告。77歳女性、23歳男性、55歳男性、76歳男性、61歳男性。COVID-2019の症状が出てから5-10日後に発症。抗ガングリオシド抗体は3例で陰性、2例で未検。MRIでは神経根や脳神経の造影効果がみられた。全例髄液SARS-CoV-2のPCRは陰性。軸索型3例、脱髄型2例。治療はIVIg (1例で血漿交換追加) が行われ、4週間後の予後は、2例がICU、2例が神経症状のためリハビリ継続、1例が独歩退院。
この報告をみると軸索型、脱髄型も同じくらい起こしうるのでしょうか。それぞれの臨床経過は、他の感染症に伴うGuillain-Barre症候群と比べて大きくは違わなさそうな印象です。これまでの症例で、抗ガングリオシド抗体が検出されたとの報告はなく、抗体との関連は気になる所です。
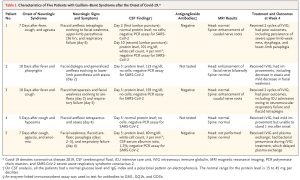
⑤Miller Fisher syndrome and polyneuritis cranialis in COVID-2019 (Neurology, 2020.4.17 published online)
2例報告。眼筋麻痺を含む末梢神経障害。50歳男性、39歳男性。1例目は、2日間垂直性複視、口周囲のしびれ感、歩行障害で受診。受診5日前にCOVID-19の症状。抗GD1b抗体陽性。SARS-CoV-2のPCRは咽頭で陽性、髄液で陰性。IVIgで改善。2例目は複視で受診。3日前から下痢などCOVID-19の症状。SARS-CoV-2のPCRは咽頭で陽性、髄液で陰性。対症療法で帰宅し、telemedicineでの経過観察となった。そのため、抗ガングリオシド抗体は提出せず。1例目では抗体が検出されているので、ウイルスによる障害よりも免疫学的機序が想定される。Miller Fisher syndromeは抗GQ1b抗体が有名だが、抗GQ1b抗体陽性よりも、抗GD1b抗体陽性の方が回復は早いことが知られているとのこと。
Guillain-Barre症候群を起こすのなら、当然Fisher症候群も起こるのでしょう。抗GQ1b抗体ではなく、抗GD1b抗体だったというのが興味深いです。
⑥Guillain-Barré syndrome following COVID-19: new infection, old complication? (J Neurol, 2020.4.24 published online)
症例は70歳女性。3月28日に、1日以内に進行する脱力感、四肢感覚障害、歩行障害で救急外来を紹介受診。彼女は3月4日に発熱 (38.5℃) の発熱、乾性咳嗽があり、1日後に鼻咽頭から採取した検体でSARS-CoV-2-RNAのRT-PCRが陽性だったが、それは数日で軽快していた。
救急外来では、胸部CTですりガラス陰影がみられたが、SpO2 98%で採血検査でも好中球優位の白血球増加のみであった。鼻咽頭のSARS-CoV-2-RNAを再検したが陰性だった。3月31日の髄液検査では、細胞数 1 /ulと正常範囲内で、蛋白48 mg/dlと軽度上昇していた。神経伝導検査が行われ、患者はGuillain-Barre症候群と診断された (神経伝導検査の結果をみると脱髄型 (AIDP) と考えられる)。免疫グロブリン大量静注療法が開始された。4月1日に挿管され、人工呼吸器管理となった。抗ガングリオシド抗体は検索されなかった。
とにかく早く報告することを意識していたのか、治療を開始したところで報告が終わっています。他の疾患の除外が不十分と考察されているが、臨床的にはGuillain-Barre症候群でほぼ間違いはないでしょう。
⑦Guillain-Barre syndrome related to COVID-19 infection (Neurology, 2020.4.28 published online)
症例は71歳男性。亜急性の経過で四肢の感覚障害、次いで3日前から急速に進行する四肢遠位の弛緩性麻痺を発症し、救急外来に紹介されてきた。前の週に、彼は微熱が数日間続いていた。既往歴は高血圧症、腹部大動脈瘤、肺癌術後があったが、神経疾患はなかった。神経学的には、四肢筋力低下及び感覚障害、腱反射消失がみられた。室内気でPaO2 65 mmHgの低酸素血症があった。胸部CTではすりガラス影やconsolidationがあり、COVID-19に典型的だった。鼻咽頭ぬぐいでは、SARS-CoV-2が陽性だった。髄液は細胞数9 /ulと軽度の細胞数増多があり、蛋白 54 mg/dlと上昇していた。髄液のSARS-CoV-2は陰性だった。神経伝導検査を行い、脱髄型Guillain-Barre症候群と診断した。入院数時間後から免疫グロブリン大量静注療法を行った。非再呼吸式マスクでの60-80%酸素投与、抗ウイルス療法 (ロピナビル+リトナビル)、ヒドロキシクロロキン投与を行った。しかし入院24時間で呼吸不全が進行し、CPAP導入、腹臥位療法を行った。しかし、患者は数時間後に呼吸不全で死亡した。
ミラノからの報告。考察に “Early respiratory support, including ICU admission, is indicated but not always feasible during the current pandemic” と書いてあり、医療が崩壊しているイタリアの状況が伝わってきます。抗ガングリオシド抗体がどうのとかは言ってられない状況のようです。